2026年2月9日,武汉大学药学院董长江教授课题组、郭锋彪教授课题组、张郑宇老师课题组与四川大学董浩浩研究员课题组合作,在国际著名学术期刊《NatureCommunications》上发表了题为“Molecular mechanism of action of small molecule SMT-738 on bacterial lipoprotein transporter LolCDE”的最新研究成果。该研究利用冷冻电镜等技术首次在原子分辨率水平揭示了小分子化合物抑制革兰氏阴性菌外膜脂蛋白转运复合物LolCDE功能的分子机制。
外膜脂蛋白是革兰氏阴性菌外膜的重要组成成份之一,也是细菌维持环境适应性、耐药性和致病性的必要条件,其转运与成熟依赖于LolABCDE复合物。ABC转运体LolCDE从内膜中提取脂蛋白,并将其转移至伴侣蛋白LolA。LolA携带脂蛋白穿越细菌周质空间抵达外膜。随后,LolB将脂蛋白锚定在外膜上。鉴于LolCDE复合物在外膜脂蛋白转运过程中的重要作用,其被认为是最重要的抗菌靶标之一。目前通过遗传学方法已经鉴定出若干种靶向LolCDE复合物的小分子抑制剂(如:SMT-738),然而这些小分子对LolCDE复合物的作用分子机制未知,从而阻碍了针对LolCDE的抗菌化合物的进一步研发。
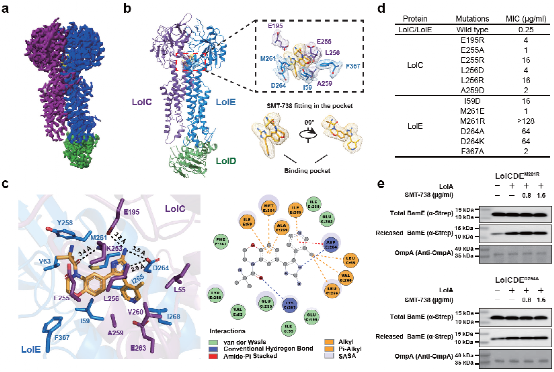
本研究利用单颗粒冷冻电镜技术,成功解析了LolCDE-SMT-738复合物的高分辨率结构。结构分析发现小分子SMT-738结合在LolCE跨膜结构域的周质端,且结构中仅有一个与LolE结合的ATPase LolD亚基存在,而与LolC相互作用的LolD亚基丢失。在所获得的结构基础上,本研究通过突变耐药性测试、生化实验及分子动力学模拟进一步验证科学猜想,最终我们提出了SMT-738的作用模型如下:小分子SMT-738结合引发了LolCE跨膜结构域及coupling helix结构域的构象变化,导致一个LolD亚基从LolCDE复合物中解离。该结构破坏使得LolCDE复合物陷入“锁死”状态,丧失转运能力。
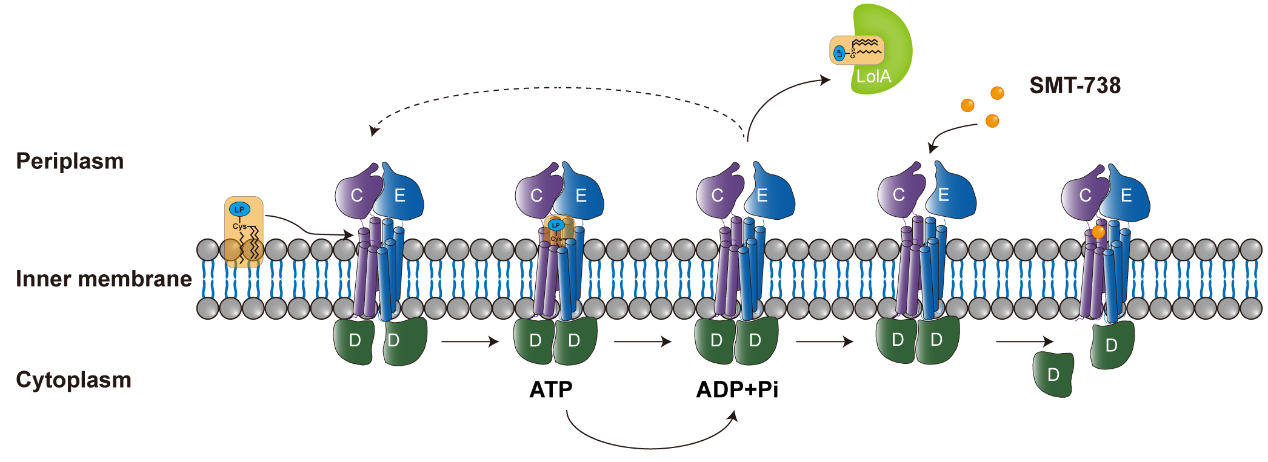
此外,我们的研究结果也初步阐明了SMT-738的耐药机制及其选择性作用于肠杆菌科细菌的机制。综合而言,该研究能为革兰氏阴性菌LolCDE抑制剂的设计提供数据支持,具有重要的研究意义。
致谢
武汉大学药学院董长江教授、郭锋彪教授、张郑宇老师和四川大学董浩浩研究员为论文通讯作者,武汉大学药学院博士后李昊天、博士研究生朱潇静和张冬冬为论文共同第一作者。药学院为文章第一完成单位。该研究得到了中国国家重点研发计划(2022YFA1303500,2021YFA1301900)、国家自然科学基金(项目编号:32250710142)、四川省自然科学基金杰出青年科学家基金项目(2024NSFJQ0002)、武汉大学战略与人才支持计划以及中央高校基础科研基金和国家自然科学基金(项目编号:32370696)的支持。感谢武汉大学科研公共服务平台冷冻电镜机组实验员李香凝的协助,感谢武汉大学药学院周海兵教授的协助。
文章信息:https://www.nature.com/articles/s41467-026-69411-2