近日,国际权威期刊《自然·化学》(Nature Chemistry)以News & Views(新闻与观点)形式发表了题为“Dual-enzyme logic powers azetidine biosynthesis”的特别评述,对武汉大学药学院、中南医院药学研究院陈文青教授课题组、张郑宇副教授课题组与厦门大学王斌举教授课题组前期联合完成的突破性研究进行了深度解读和高度评价。该评述充分肯定了联合团队在氮杂环丁烷类药效团生物合成机制研究中取得的重要成果。
氮杂环丁烷作为药物研发领域的“明星药效团”,在抗肿瘤、抗病毒等药物设计中具有不可替代的价值。然而,该结构高达约25 kcal/mol的环张力,使其化学合成需依赖预活化底物、多重保护基或剧烈反应条件,故极大限制了其在药物研发中的广泛应用。自然界中含氮杂环丁烷结构的天然产物如何在温和条件下完成这一高能垒转化,已成为长期科学之谜。前期联合团队率先破解了氮杂环丁烷生物合成的“双酶协同”逻辑,即:金属酶PolE与PolF以L-异亮氨酸为起始底物,通过级联反应高效构建氮杂环丁烷。相关成果以“A two-metalloenzyme cascade constructs the azetidine-containing pharmacophore”为题发表于《Nature Chemistry》(DOI: 10.1038/s41557-025-01949-y)。
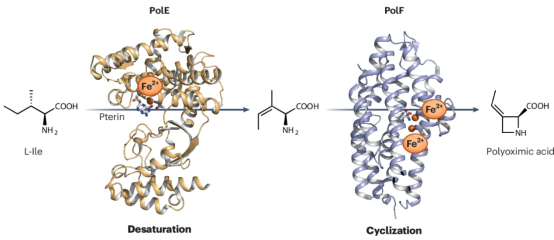
评述高度认可相关研究的科学价值与创新意义,指出:PolE作为Fe²⁺/蝶呤依赖型酶家族(DUF6421)的新成员打破了该类酶传统的羟化催化模式,并发现PolE与蝶呤辅因子直接配位确保了底物的高选择性活化,进而成为整个合成通路的“效率推进器”;同时指出:PolF通过七螺旋结构精准将底物定位于双铁簇活性中心,并通过氧激活、氢攫取及自由基重排等系列反应,从而实现氮杂环丁烷的高效构建。此外,评述进一步强调了联合团队发现的“双酶协同”驱动四元环合成的全新生物催化逻辑,并惊叹:相关发现不仅破解了该领域悬而未决的机制难题,更为未来实现高价值氮杂环丁烷类药物的生物制造与分子设计开辟了全新路径。
展望未来,联合团队期望进一步拓展双酶系统的底物谱,并深入探索其功能多样性延伸的分子酶学机制,进而为开发更高效的生物催化剂提供理论支撑,同时有效助力我国微生物药物合成生物学的技术突破与产业升级。
评述链接:https://www.nature.com/articles/s41557-026-02079-9