孕期用药安全始终是医学界和公众关注的焦点。孕妇在孕期接触各种药物(如糖皮质激素、解热镇痛药、咖啡因等)的情况十分普遍,这些药物对胎儿神经发育的潜在影响是公共卫生和临床医学关注的重大课题。武汉大学药学院徐丹教授团队依托组合生物合成与新药发现教育部重点实验室以及发育源性疾病湖北省重点实验室,长期致力于这一领域的研究,近期在一系列系统性工作中取得突破,不仅揭示了多种常见药物损害子代神经发育的共同机制,还成功构建了一套创新毒性筛查技术,为药物发育毒性的安全性评价提供了新思路。
团队的前期研究以临床常用的人工合成类糖皮质激素地塞米松为模型,开展了机制层面的深入探索。发表于环境健康领域权威期刊Environment International(链接:https://doi.org/10.1016/j.envint.2024.109064)的研究首次清晰勾勒出地塞米松导致子代神经损伤的完整通路:药物激活糖皮质激素受体后,促使microRNA-450a-3p表达上升,进而抑制组蛋白乙酰转移酶HAT1,最终降低胆固醇转运蛋白ABCG1的表达。这一连串分子事件导致星形胶质细胞向神经元运输胆固醇的过程受阻,进而引发突触形成障碍与认知情感缺陷。该研究精准定位了ABCG1这一关键靶点,为后续研究奠定基础。
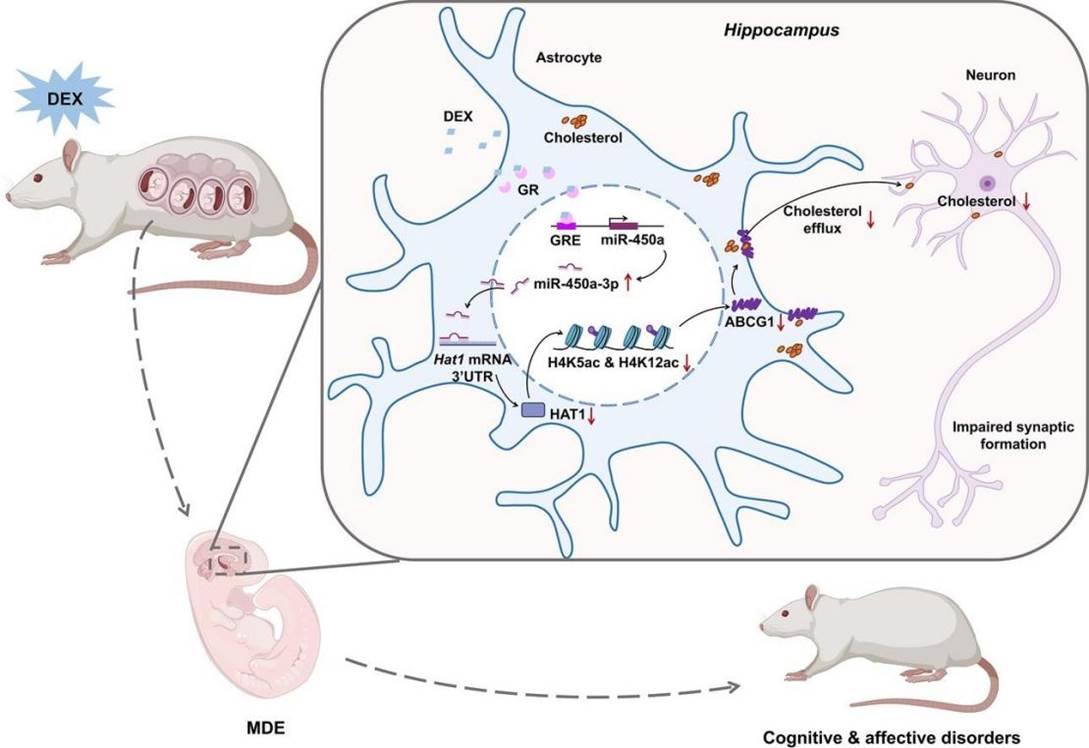
Environment International 2024
Graphical Abstract: Abnormal GR/miR-450a-3p/HAT1/ABCG1 signaling axis causes long-term cognitive and emotional neurobehavioral changes in prenatal dexamethasone exposed-offspring by blocking cholesterol efflux in hippocampal astrocytes.
在明确地塞米松的作用机制后,团队进一步思考:ABCG1所介导的胆固醇稳态失调是否也是其他药物引发神经毒性的共同途径?近期发表在代谢研究领域权威期刊Metabolism: Clinical and Experimental(链接:https://doi.org/10.1016/j.metabol.2025.156454)上的研究将目光转向咖啡因。该研究进一步阐释,咖啡因通过激活母体下丘脑-垂体-肾上腺轴,升高内源性糖皮质激素水平,进而引发海马区内“GR–miR-130b/301b–PPARg–ABCG1”这一信号轴的级联反应,最终精准影响ABCG1的功能。尽管咖啡因与地塞米松在结构和药理上差异显著,但研究显示,咖啡因同样通过母体应激轴引发信号级联反应,最终影响ABCG1功能,导致神经发育异常。这一发现提示,“通过ABCG1扰乱胆固醇转运”可能是不同药物诱发神经发育毒性的共性机制。
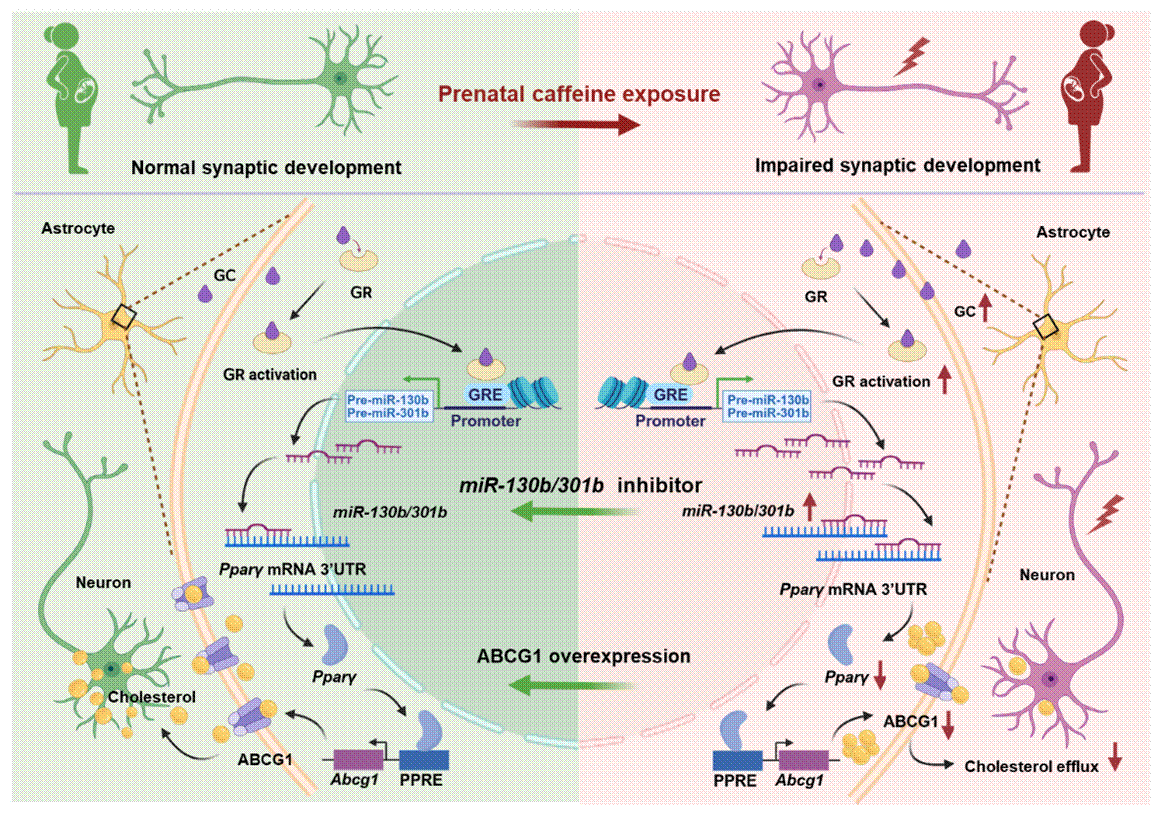
Metabolism: Clinical and Experimental 2026
Graphical Abstract: Prenatal caffeine exposure activates maternal-fetal glucocorticoid signaling, disrupting astrocyte-neuron cholesterol homeostasis and impairing hippocampal synaptic development via the GR-miR-130b/301b-Pparγ-ABCG1 axis.
机制的揭示为工具开发铺平了道路。在近期作为封面文章发表于环境科学与技术领域顶尖期刊Environmental Science & Technology(链接:https://doi.org/10.1021/acs.est.5c04496)的工作中,徐丹团队实现了从理论到应用的跨越。研究利用斑马鱼模式动物不仅进一步证实了地塞米松、泼尼松、对乙酰氨基酚、阿莫西林、阿奇霉素等多种药物均能一致抑制abcg1表达,更据此构建了Tg(abcg1:EGFP)转基因斑马鱼模型。该模型如同一个“生物传感器”,能够通过荧光信号实时、直观地反映abcg1表达变化,快速识别具有神经发育毒性的化合物。这项工作不仅为药物神经发育毒性的安全性评价提供了灵敏、可靠的高通量筛查技术,其基于保守机制的设计原理,也使其在评估更广泛的环境污染物(如持久性有机污染物、内分泌干扰物等)的神经发育毒性方面展现出巨大的应用潜力。
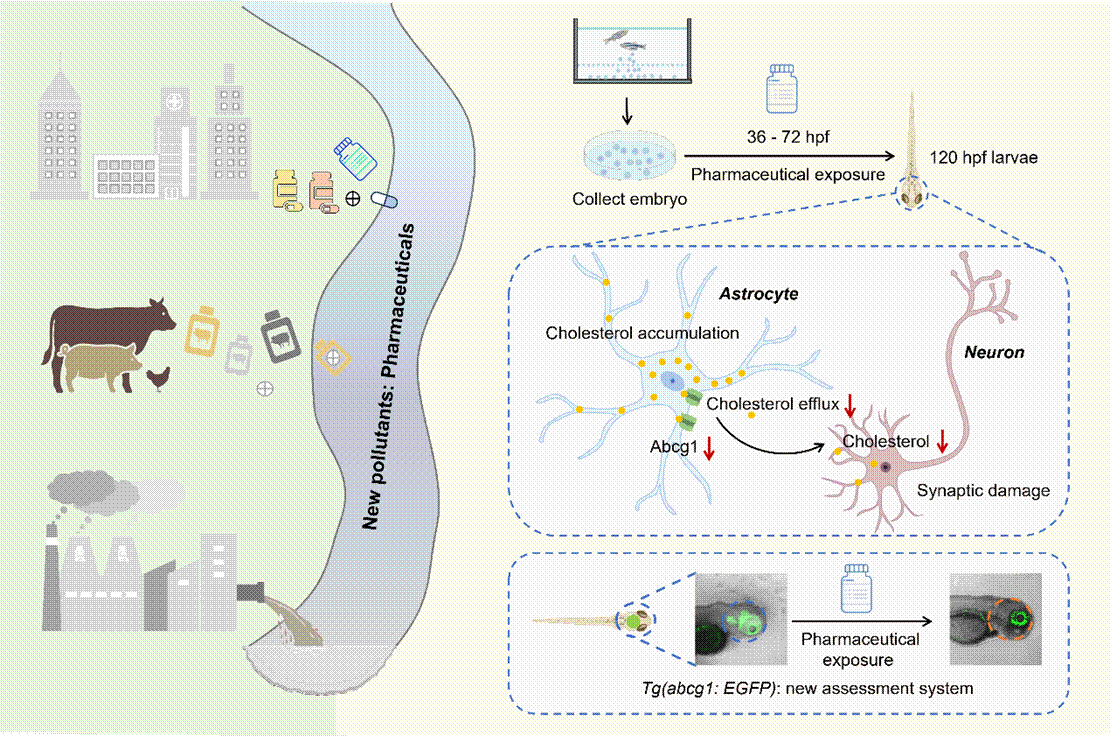
Environmental Science & Technology 2025
Graphical Abstract: Cholesterol Homeostasis Disruption as a Mechanism of Pharmaceutical-Induced Neurodevelopmental Toxicity: A Transgenic Zebrafish Screening Model Based on abcg1.
基于上述系列研究成果,团队的探索仍在持续深化。目前,研究工作正沿着两个方向进一步延伸:一是探索将“脑内胆固醇稳态”这一核心机制发展为可应用于临床的外周预警标志物;二是基于该机制探索可能的靶向干预策略,为主动预防药物相关的神经发育障碍开辟新的路径。这些持续性的探索,有望为相关神经发育障碍的监测与预防提供新思路。
徐丹教授团队的系列工作,从地塞米松的精细机制解析出发,逐步揭示多种药物的共性作用通路,并最终研发出实用性筛查工具,不仅深化了对药物神经发育毒性机制的理解,也为孕期安全用药和环境风险评估提供了重要科学依据与技术支撑。
本系列研究成果的取得,离不开研究团队成员的紧密协作与多方支持。在发表于Environment International、Metabolism与Environmental Science & Technology的系列论文中,徐丹教授作为独立通讯作者统筹并指导了全部研究工作。博士研究生代高乐、骆名翠以及硕士研究生戴诗韵、周昕丽等作为主要贡献者,在不同研究中承担了关键任务,分别为相关论文的共同第一作者。整个系列工作始终得到发育源性疾病湖北省重点实验室主任汪晖教授的悉心指导,并获得了张瑞霖教授在斑马鱼模型构建、中国科学院水生生物研究所段明研究员在技术平台方面的重要支持。此外,本研究系列还受益于国家重点研发计划、国家自然科学基金及湖北省自然科学基金等多个国家级与省部级项目的持续资助。
撰写:代高乐、徐丹