近日,武汉大学药学院刘鑫团队联合华中科技大学杨帆团队在国际权威期刊《Advanced Science》发表题目为“Engineered Dual-Function Antibody-Like Proteins to Combat SARS-CoV-2-Induced Immune Dysregulation and Inflammation”的文章,该杂志为中科院1区,2025年最新影响因子14.1。SARS-CoV-2对人类健康的威胁不仅限于呼吸系统损伤。它还通过免疫系统过度激活,尤其是补体系统异常反应,导致免疫失调,这一现象已成为致命性疾病的重要因素。为应对这一挑战,团队开发两种新型抗体样蛋白——Lectifitin-36与Lectifitin-41,成功缓解了由SARS-CoV-2引起的免疫系统异常。
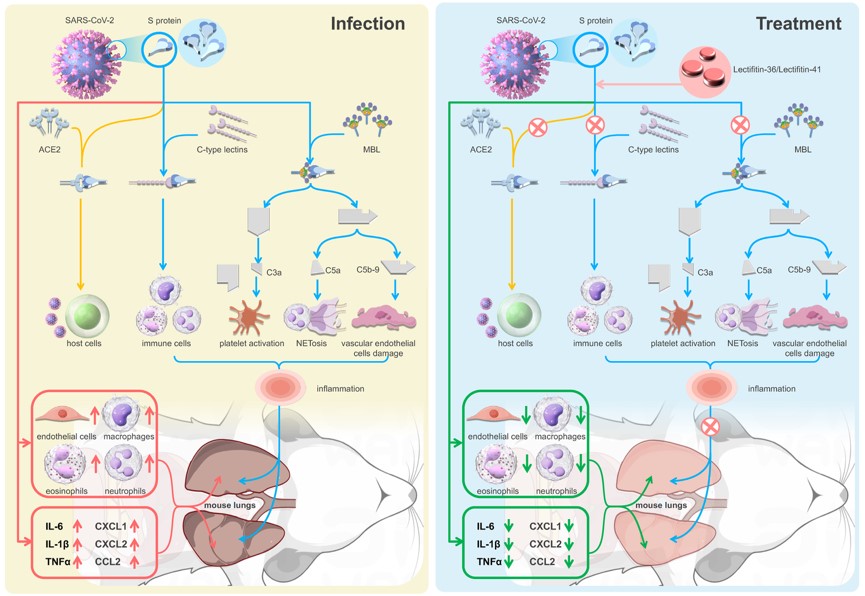
SARS-CoV-2的刺突(S)蛋白是病毒与宿主细胞表面ACE2受体以及多种C型凝集素相互作用的关键因子。病毒通过S蛋白与ACE2受体和C型凝集素的结合启动宿主免疫反应。然而,这一过程中,补体系统的异常激活及免疫细胞的过度聚集,特别是中性粒细胞胞外诱捕网(NETs)的形成,导致了急性肺损伤、呼吸窘迫综合症(ARDS)等严重病理表现。研究表明,这种免疫失调与SARS-CoV-2感染的病理变化密切相关,是导致新冠重症和死亡的核心因素。
为应对由SARS-CoV-2引发的免疫失调, 研究团队设计了两种抗体样蛋白——Lectifitin-36与Lectifitin-41。这两种蛋白基于人类甘露糖结合凝集素(MBL)和ACE2受体模拟肽,通过cDNA展示技术优化,能够特异性地结合SARS-CoV-2的S蛋白。
Lectifitin-36与Lectifitin-41的独特之处在于其“双重机制”。它们不仅能通过竞争性抑制S蛋白与ACE2受体的结合,阻止病毒进入宿主细胞,还能够有效抑制S蛋白与免疫细胞表面C型凝集素的结合,从而减少免疫系统的过度激活和补体系统的异常反应。该实验结果为新冠病毒及其变异株的治疗提供了新的思路。

研究成果标志着新冠免疫治疗领域的一项重要突破,这些抗体样蛋白通过双重靶向机制,既能够抑制SARS-CoV-2与宿主细胞的结合,又能有效调节由病毒引发的免疫失调,减少免疫过激反应导致的组织损伤。与传统单靶向疗法相比,Lectifitin-36与Lectifitin-41展现了更为广泛的治疗潜力。
刘鑫教授团队长期致力于抗肿瘤及抗病毒药物研发,为本研究提供了重要的理论及实验支持。该文章的共同第一作者是武汉大学药学院本科生王一卓和2022级硕士研究生白辰午,刘鑫教授、华中科技大学杨帆教授为共同通讯作者,武汉大学药学院为第一完成单位。文章还得到了武汉大学A3病毒实验室、武汉大学仪器共享平台、华中科技大学等科研机构的大力支持,文章受到国家自然科学原创探索基金及面上基金,武汉大学医学部2020地素爱未来科研项目及2024重点教研项目的资助。感谢武汉大学国家重点实验室陈宇教授,刘乾运博士,武汉大学泰康医学院龚克教授,罗志鸿博士,华中科技大学研究生浦凡,武汉大学药学院鲁丽特聘研究员,艾时斌博士等老师为本研究提供支持和帮助。
论文链接:https://pubmed.ncbi.nlm.nih.gov/40619617/